
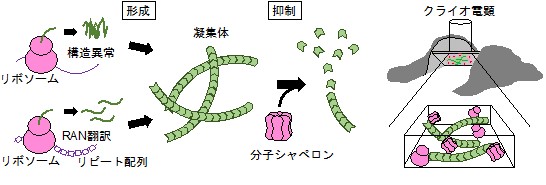
筋萎縮性側索硬化症(ALS)、パーキンソン病、アルツハイマー病、ハンチントン病といった神経変性疾患は、細胞内で異常タンパク質が線維状の凝集体(アミロイド)を形成し蓄積されることが原因と考えられている。近年、リピート関連性非ATG依存性(RAN)翻訳によるリピート配列の異常伸長とそれに起因する凝集体の形成や、分子シャペロンによるアミロイドの脱凝集といった興味深い現象が明らかとなっている。我々は最近、クライオ電子顕微鏡を用いて家族性アルツハイマー病の変異をもったアミロイド線維の高分解能構造解析に成功した(未発表)。本研究では細胞内で形成される凝集体と、その形成・抑制を司るリボソームや分子シャペロンに注目し、それらの細胞内での立体構造やお互いの空間的配置をクライオ電子線トモグラフィー法によって明らかにする。凝集体とリボソームや分子シャペロンをそれぞれ異なる蛍光で標識し、光・電子相関顕微鏡(CLEM)による同定とクライオ集束イオンビーム加工(cryo-FIB milling)による薄層(ラメラ)加工の後、クライオ電子線トモグラフィー法によって細胞内での構造を解析し、凝集体の形成と抑制のメカニズムの解明を目指す。
- #Bracun L, #Yamagata A, Christianson B.M., Terada T, Canniffe D.P., Shirouzu M & *Liu, L.N. (#equally contributed) Cryo-EM structure of the photosynthetic RC-LH1-PufX supercomplex at 2.8-Å resolution. Sci. Adv. 7 eabf8864 (2021)
- Yoshida T, Yamagata A, Imai A, Kim J, Izumi H, Nakashima S, Shiroshima T, Maeda A, Iwasawa-Okamoto S, Azechi K, Osaka F, Saitoh T, Maenaka K, Shimada T, Fukata Y, Fukata M, Matsumoto J, Nishijo H, Takao K, Tanaka S, Okabe S, Tabuchi K, Uemura T, Mishina M, Mori H, *Fukai S. Canonical versus non-canonical transsynaptic signaling of neuroligin 3 tunes development of sociality. Nat. Commun. (2021) doi: 10.1038/s41467-021-22059-6
- #Wakita M, #Yamagata A, Shiroshima T, Izumi H, Maeda A, Sendo M, Imai A, Kubota K, Goto-Ito S, Sato Y, Mori H, Yoshida T, *Fukai S. (#equally contributed) Structural insights into selective interaction between type IIa receptor protein tyrosine phosphatases and Liprin-α. Nat. Commun. (2020) doi: 10.1038/s41467-020-14516-5
- Yamagata A, Goto-Ito S, Sato Y, Shiroshima T, Maeda A, Watanabe M, Saitoh T, Maenaka K, Terada T, Yoshida T, *Uemura T, *Fukai S. Structural insights into modulation and selectivity of transsynaptic neurexin–LRRTM interaction. Nat. Commun. (2018) doi: 10.1038/s41467-018-06333-8.
- Yamagata A, Miyazaki Y, Yokoi N, Shigematsu H, Sato Y, Goto-Ito S, Maeda A, Goto T, Sanbo M, Hirabayashi M, Shirouzu M, Fukata Y, *Fukata M, *Fukai S. Structural basis of epilepsy-related ligand-receptor complex LGI1-ADAM22. Nat. Commun. (2018) doi: 10.1038/s41467-018-03947-w.
- Goto-Ito S, Yamagata A, Sato Y, Uemura T, Shiroshima T, Maeda A, Imai A, Mori H, Yoshida T, *Fukai S. Structural basis of trans-synaptic interaction between PTPδ and SALMs for inducing synapse formation. Nat. Commun. (2018) doi:10.1038/s41467-017-02417-z
- Yamagata A, *Yoshida T, Sato Y, Goto-Ito S, Uemura T, Maeda A, Shiroshima T, Iwasawa-Okamoto S, Mori H, Mishina M, *Fukai S. Mechanisms of splicing-dependent trans-synaptic adhesion by PTPδ–IL1RAPL1/IL-1RAcP for synaptic differentiation. Nat. Commun. (2015) doi:10.1038/ncomms7926
- Yamagata A, Sato Y, Goto-Ito S, Uemura T, Maeda A, Shiroshima T, Yoshida T, *Fukai S. Mechanisms for splicing-dependent regulation of trans-synaptic adhesion revealed by the crystal structure of the Slitrk2–PTPδ. Sci. Rep. (2015) doi:10.1038/srep09686
- #Kubota K, #Yamagata A, Sato Y, Goto-Ito S, *Fukai S. (#equally contributed) Get1 stabilizes an open dimer conformation of Get3 ATPase by the binding at two distinct interfaces. J. Mol. Biol. 422, 366-375 (2012)
- Yamagata A, Mimura H, Sato Y, Yamashita M, Yoshikawa A, *Fukai S. Structural insight into the membrane insertion of tail-anchored proteins by Get3. Genes to Cells 15, 29-41 (2010)

